Врачи могут имитировать операции на сердце одним щелчком мыши
Сядьте на борт самолета, и вы можете быть уверены, что он прошел строгие испытания на безопасность перед своим первым полетом и, по сути, еще до того, как был построен. Вы можете быть уверены, что инженерное программное обеспечение провело поиск по широкому диапазону конструктивных параметров, чтобы найти наиболее аэродинамическую форму, самые гладкие крылья, самый прочный фюзеляж. Конкурирующие конструкции прошли «тестовые полеты» в компьютерном моделировании, чтобы предсказать, как они будут вести себя как в дружественном, так и в неспокойном небе.

Пойдите в больницу для проведения операции на открытом сердце, и ваш врач разработает для вас лечение, используя совершенно другой процесс. Скорее всего, хирург рассмотрит, какие методы лечения лучше всего работают у пациентов с симптомами, похожими на ваши, а затем применит комбинацию медицинских протоколов и интуиции, чтобы принять решение в вашем случае. Врачи могут оценить риски и преимущества процедуры, посмотрев, насколько хорошо она прошла в прошлом, но они не могут гарантировать результат в вашем конкретном случае. Несмотря на передовые диагностические инструменты и новые лекарства, медицина остается тем, чем она всегда была: эмпирической наукой.
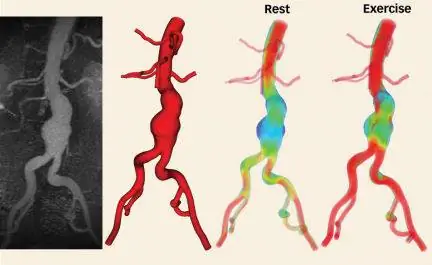
Чарльз Тейлор, профессор биоинженерии Стэнфордского университета, хочет сделать подготовку к операции на сердце более похожей на конструкцию самолета. Его команда создала симулятор SimVascular, который преобразует данные магнитно-резонансной томографии (МРТ) в компьютерную геометрическую модель кровеносных сосудов пациента. Модель дает хирургам возможность протестировать различные хирургические процедуры и другие методы лечения, чтобы определить, какой подход лучше всего подходит для физиологии конкретного пациента.
“Пациенту делают только одну операцию. Вы не можете сделать два и посмотреть, что лучше», - говорит Тейлор. Однако, используя эту модель, хирурги могли выполнять несколько виртуальных операций и проверять идеи, даже не прикасаясь к пациенту.
SimVascular, работа над которым длилась более десяти лет, должна быть выпущена 31 августа в виде программного обеспечения с открытым исходным кодом, бесплатно доступного для исследователей во всем мире. Команда Тейлора, состоящая из кардиологов, хирургов и других специалистов, уже использует это программное обеспечение для проведения фундаментальных исследований ценности различных методов лечения сердца. Для одного типа серьезного врожденного порока сердца команда даже использовала программное обеспечение для разработки и тестирования совершенно новой хирургической процедуры. В ближайшие месяцы хирурги из Стэнфорда надеются провести эту операцию впервые.
«Это совсем другой взгляд на медицину, когда инженерия и математика внедряются в процесс планирования операции», - говорит Тейлор.
Захват тиража
В течение нескольких десятилетий исследователи моделировали физику системы кровообращения человека. В последние годы они отошли от традиционных моделей «стекло-вода» к компьютерным моделям, в которых для решения уравнений гидромеханики используются программные инструменты, унаследованные от аэрокосмической промышленности. Эти модели предоставили убедительные доказательства того, что простые гидромеханические силы, такие как кровяное давление и напряжение сдвига, лежат в основе большинства сердечных заболеваний, от накопления жировых бляшек в артериях до ослабления стенок сосудов, называемого аневризмами.
Хотя такие компьютерные модели оказались весьма информативными, они остаются идеализированными описаниями общей системы кровообращения. Индивидуальные системы кровообращения сильно различаются не только по расположению бляшек и ширине сосудов, но и по тому, как различные сосуды соединяются друг с другом.
Будучи аспирантом в начале 1990-х годов, Тейлор понял, что должна быть возможность реконструировать физиологию конкретного пациента по трехмерным изображениям кровеносных сосудов, которые создает МРТ. Сначала Тейлор планировал использовать такие модели для конкретных пациентов просто для продолжения изучения связи между механикой жидкости и здоровьем сосудов.
«Но в какой-то момент, - говорит он, - я понял, что есть гораздо более важное применение: помочь предсказать исход операции».
Стандартные программные средства гидромеханики не были предназначены для изучения кровотока, поэтому Тейлор знал, что они не подходят для его целей. Кровеносная система человека отличается от сети труб, объясняет он. Например, кровь пульсирует импульсами, а не течет плавно, а кровеносные сосуды, в отличие от труб, представляют собой гибкие трубки, которые расширяются и сужаются при каждом импульсе.
Что еще более усложняет, изображения, предлагаемые МРТ, в отличие от чертежей водопроводной системы, далеко не полны. Изображения МРТ могут показать все сосуды диаметром более 1 миллиметра, но это всего лишь несколько сотен из миллионов кровеносных сосудов в организме человека. Чтобы справиться с этими сложностями, Тейлор понял, что ему придется построить свою модель с нуля.
Программное обеспечение SimVascular запускается с МРТ-изображениями. Используя методы распознавания изображений, он извлекает геометрию основных кровеносных сосудов пациента - всех тех, которые достаточно велики, чтобы их можно было обнаружить с помощью МРТ. Затем программа делит геометрическую модель на миллионы крошечных фрагментов. Затем он выбирает репрезентативную точку внутри каждого фрагмента. В каждой такой точке дифференциальные уравнения управляют скоростью и давлением крови, а также динамикой стенок сосудов.
Чтобы сделать эти уравнения точными, где заканчивается модель и кровь течет в сосуды, слишком маленькие для обнаружения МРТ, команда Тейлора использовала существующие знания о фрактальной геометрии сосудистой системы для оценки артериального давления и других параметров. условия на этих концах. Эта функция, наряду с описанием гибких стенок кровеносных сосудов, отличает SimVascular от других попыток моделирования системы кровообращения, говорит Джей Хамфри, инженер-биомедик из Техасского университета A&M в Колледж-Стейшн. Тейлор и его команда используют свою систему, чтобы «хорошо предписывать, что происходит в конце, и это очень важно», - говорит Хамфри.
SimVascular использует дифференциальные уравнения для создания фильма-книжки о кровотоке в сосудистой системе. Программное обеспечение делит каждую секунду времени примерно на 10 000 шагов и использует дифференциальные уравнения для расчета сил в каждой репрезентативной точке для каждой доли секунды. Хирурги и исследователи могут просмотреть фильм и получить подробную информацию о кровяном давлении, сдвиговом напряжении и других состояниях в каждой точке кровеносных сосудов.
Создание такого фильма требует одновременного решения около 10 миллионов уравнений для каждого момента времени. В настоящее время суперкомпьютерам Стэнфордской команды требуется несколько дней, чтобы создать 20-секундный фильм, но Тейлор надеется сократить время работы до одного дня или нескольких часов. Такое ускорение уложит процесс моделирования в обычный график хирургического планирования.
Хирурги могут использовать готовую модель для проверки воздействия существующих методов лечения на данного пациента. В более широком смысле они могли бы использовать модель для тестирования «любой процедуры, которую вы можете себе представить», - говорит Тейлор. В настоящее время хирург с идеей нового типа операции может, если повезет, испытать ее на нескольких животных или трупах. Кроме того, у хирургов есть несколько вариантов, кроме проведения операции на живом, дышащем пациенте.
«Я думаю, хирургам будет проще проверять дикие идеи, которые могут оказаться хорошими», - говорит Тейлор.
Половина сердца
Команда Тейлора уже приступила к тестированию одной новой идеи, которую стэнфордские хирурги могут представить в течение нескольких месяцев. Они надеются, что это улучшит качество жизни детей, рожденных с особо серьезными пороками сердца.
Каждый год в Соединенных Штатах рождается до 1 500 детей, по сути, с половиной сердца. Нормальное сердце имеет две насосные камеры. Один, правый желудочек, перекачивает кровь в легкие для получения кислорода, а другой, левый желудочек, перекачивает обогащенную кислородом кровь по телу. Однако в редких случаях одна из этих камер не может правильно сформироваться.
До рождения этот порок развития не является проблемой, поскольку мать насыщает кислородом кровь своего ребенка, пока он находится в утробе матери. Однако, чтобы выжить после рождения, ребенку с пороком развития требуется серия процедур по перенаправлению сердечных сосудов так, чтобы одна камера могла выполнять всю необходимую перекачку. После перенаправления кровь, прошедшая через тело, направляется в легкие, прежде чем вернуться в сердце.
На протяжении десятилетий хирурги, выполняющие такое изменение маршрута, соединяли основные кровеносные сосуды в форме креста. При этой процедуре две вертикальные вены, идущие из верхней и нижней частей тела, соединяются с двумя горизонтальными артериями, несущими кровь в левое и правое легкие. Однако такая связь не очень эффективна. Кровь, текущая вниз к соединению, сталкивается лоб в лоб с кровью, текущей вверх, и возникающая в результате турбулентность тратит энергию впустую. Потеря энергии является серьезной проблемой для этих пациентов, у которых одна насосная камера должна выполнять работу двух.
«У пациентов в подростковом возрасте часто возникает сердечная недостаточность, и им требуется пересадка сердца», - говорит Элисон Марсден, исследователь из лаборатории Тейлора, которая использовала SimVascular для изучения процедуры перенаправления.
Около 10 лет назад некоторые хирурги начали проводить «офсетную» операцию, при которой верхняя вена по-прежнему соединяется в центральном соединении, а нижняя вена шунтируется в одну сторону, избегая лобового столкновения. крови. Однако эта процедура создает свой собственный набор проблем. Он доставляет больше крови в одно легкое, чем в другое, потенциально подавляя рост запущенного легкого.
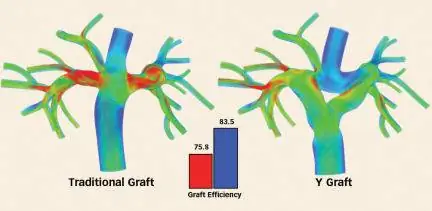
Вместе с детским кардиологом из Стэнфорда Джеффри Файнштейном Марсден и Тейлор придумали новую идею. Хирург может прикрепить Y-образный трансплантат к нижней вене, а затем соединить два коротких плеча Y с двумя горизонтальными артериями. Это создаст «съезды с шоссе», - говорит Тейлор. «С точки зрения гидромеханики это имело большой смысл».
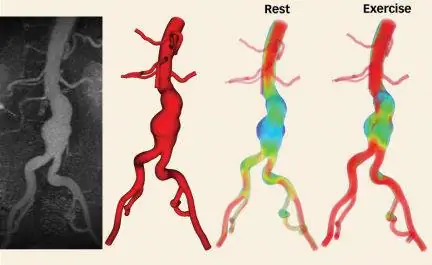
Программное обеспечение SimVascular позволило команде сравнить прогнозируемую эффективность Y-графта с эффективностью офсетного трансплантата. Более ранние исследования предполагали, что процедура смещения эффективна на 90 процентов, что врачи считают хорошим результатом. Однако эти исследования были ограничены тем фактом, что тесты на эффективность сердца пациента обычно проводятся, когда пациент находится в состоянии покоя. На основании этой информации врачам трудно предсказать, как пациент будет себя вести во время активной деятельности.
«Измерения, которые мы проводим, всегда проводятся на лежащих детях, но они не так проводят свои дни», - говорит Файнштейн.
SimVascular, однако, может легко имитировать условия упражнений. Тренажер просто увеличивает частоту сердечных сокращений и приток крови к основным работающим мышцам, уменьшает приток крови к таким органам, как желудок и почки, и регулирует некоторые другие параметры, которые обычно меняются во время активности.
Моделирование Марсдена показало, что во время упражнений эффективность офсетного трансплантата падает до 65-70 процентов, тогда как эффективность Y-графта составляет 80 процентов. Во время отдыха Y-графт работает с эффективностью 95 %, что также превосходит показатели офсета.
Когда хирурги, сотрудничающие с Тейлором и Файнштейном, увидели цифры, они очень хотели попробовать новую процедуру, и команда надеется сделать это возможным в ближайшие месяцы. «Хирурги были готовы попробовать это раньше нас, потому что именно так они и делают», - говорит Файнштейн.
Новый взгляд на болезни сердца
В дополнение к проекту Y-графта команда Тейлора использует SimVascular для изучения множества других сердечных заболеваний и методов лечения, от изучения того, замедляют ли упражнения рост аневризм аорты, до изучения кровотока у здоровых людей. детей сравнивается с таковой у детей, рожденных с выраженным сужением аорты.
Опираясь на свой опыт работы в аэрокосмической технике, Марсден использовала методы оптимизации, чтобы определить наилучшее место и угол, под которым хирург должен прикрепить аортокоронарное шунтирование. Аортокоронарное шунтирование - это типичная «операция на открытом сердце», которую делают людям с сильно закупоренными сердечными артериями, вызывающими боль в груди и угрожающими сердечными приступами.
Этот процесс «похож на проектирование крыла самолета, в котором вы смотрите, как изменение формы влияет на подъемную силу и сопротивление», - говорит она. «Здесь мы спрашиваем, как форма трансплантата влияет на поток и напряжение сдвига», силу трения крови о стенки сосуда.
В другом исследовании ученые пришли к некоторым выводам о вариантах лечения высокого кровяного давления в артериях легких, известного как легочная гипертензия. От 50 000 до 100 000 человек в Соединенных Штатах страдают от легочной гипертензии, и в наиболее тяжелых случаях она приводит к сердечной недостаточности и смерти. Беверли Танг, аспирант лаборатории Тейлора, использовала модели SimVascular пациентов с легочной гипертензией, чтобы рассчитать, как их высокое кровяное давление влияет на напряжение сдвига. Невозможно измерить напряжение сдвига с помощью обычных диагностических инструментов. «Программное обеспечение позволяет нам получать информацию, которую мы не можем получить в клинике», - говорит Файнштейн.
Напряжение сдвига играет важную роль в здоровье сосудов, потому что силы трения, создаваемые приливом крови, стимулируют нормальный рост и развитие клеток, выстилающих кровеносные сосуды. Группа Тейлора обнаружила, что в областях с низким напряжением сдвига в аорте, как правило, скапливаются бляшки.
«Это одна из причин, по которой упражнения так полезны - они увеличивают поток и напряжение сдвига», - говорит Файнштейн.
Tang обнаружил, что, согласно моделированию SimVascular, напряжение сдвига было почти на порядок ниже у пациентов с легочной гипертензией, чем у здоровых людей. Чтобы оценить эффект этого низкого напряжения сдвига, Танг подверг вырезанные клетки стенки сосуда в лаборатории воздействию напряжения сдвига, типичного для пациентов с легочной гипертонией. Клетки воспалились, и уровень их функционирования снизился.
Высокое кровяное давление, определяющее легочную гипертензию, по-видимому, вызывает «каскад осложнений», - говорит Файнштейн. Эти эффекты могут объяснить, почему болезнь прогрессирует, что было загадкой для медицинских исследователей. Выводы Тана предполагают, что может быть уместно более агрессивно лечить ранние случаи легочной гипертензии, используя препарат под названием простациклин, который врачи обычно приберегают для тяжелых случаев. В отличие от некоторых других методов лечения, этот препарат увеличивает кровоток, тем самым повышая напряжение сдвига. Файнштейн полагает, что его использование при более легкой легочной гипертензии, чем обычно, может предотвратить каскад, ведущий к полномасштабной болезни.
«Моделирование проливает новый свет на эту болезнь», - говорит Файнштейн.
После публичного выпуска SimVascular 31 августа программное обеспечение «начнет использоваться для решения гораздо большего числа задач, чем мы можем решить самостоятельно», - говорит Тейлор. Хотя многие из этих проблем, вероятно, относятся к области фундаментальных исследований, Тейлор надеется, что некоторые исследователи превратят программное обеспечение в еще более мощный инструмент, который поможет врачам и хирургам решать, как лечить конкретных пациентов.
«Инженеры считают само собой разумеющимся, что вы построите теоретическую модель и будете использовать ее для предсказаний, но медицина не развивалась таким образом, потому что тела и болезни настолько сложны», - говорит Тейлор. «Но теперь, - добавляет он, - когда я рассказываю об этом подходе врачам, они говорят: «Вау, конечно, это надо делать».